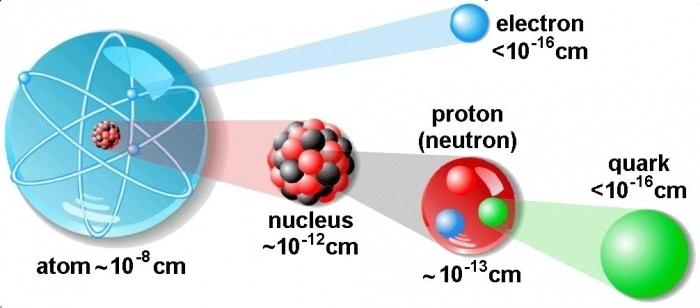
同位体は、核の組成における化学元素の異なるタイプである
人間の記憶は連想論理接続。したがって、現実を合理化し、細胞によってその要素を分配し、システムを見つけることは、私たちにとって非常に重要です。そうでなければ、記憶は拒否し、心は分析する。化学の歴史の中で偶然ではありません。そのような重要な画期的な進歩は、周期表の作成です。順序、システム、論理が勝利を収めました。この発見の影響は大きかったので、多くの人にインスピレーションを与えました。たとえば、ロシアの時間管理の天才であるLyubishchevは、生物の周期表を作成するために自分のシステムを開発しました。この目標は達成されませんでしたが、事実自体は人間の理解のための論理の重要性を証明します。しかし、現実は美しい計画よりも豊かです。たとえば、化学のメインテーブルでは、いくつかの要素が質量の順序に違反しています。なぜ?あなたは1つの単語に答えることができます - "同位体"。この言葉は文字どおり「占有する」という意味です。

多くは働いて、すべてを覚えていない
メンデレーエフのテーブルは骨の折れる仕事の成果です創造者だけでなく、多くの科学者。彼は素晴らしく原理そのものを作り、基本パターンを見つけました。しかし、あなたが各要素の下で見る質量の数字 - 多くの化学者の仕事の成果、さらにそれは不正確です。これはどうやってできますか?原子番号がきれいな整数であることに気がついたことでしょう。しかし、質量は小数であり、小数点以下の桁数は非常に多い。なぜ?そして、同じ同位体は責任を負うべきです。これは非常に簡単に説明されています。 「窒素」元素の数字を見ると、14,0067での原子質量の数字が表示されます。しかし、遊離窒素原子を「捕まえる」とすれば、10と25の原子単位の重さができます。彼らは違う。違いは何ですか?同位体の質量は、陽子の質量と中性子の質量からなる。陽子の質量は一定の値であり、元素を窒素(窒素 - 窒素)とする。しかし、中性子の場合、原子は豊かでも貧弱でもあります。窒素を用いた例では、それらは18であり、わずか3個である。同位体は、核中の中性子の数に依存する元素原子のタイプです。 16個の窒素同位体があります。他の要素にはより多くのものがあります。
科学者は何をすべきですか?

あなたが科学者であれば、どうしますか? どのように計算のために表に質量を記録しますか?もちろん、算術平均をとることは可能でした。しかし、多くの同位体は非常に不安定なものであり、人工的に作られたものもあります。したがって、不正確なデータに基づいて計算を行うのは間違いです。科学者たちは異なって行動しました。彼らは、ある同位体の天然存在量に比例して元素の原子質量を計算しました。結果として、任意の検索で14単位の同位体が得られる可能性は非常に高くなります。偶然発見された同位体の核は、おそらく7個の陽子と7個の中性子を含むであろう。
不正確な理由

なぜ原子質量は正確ではないのですか? それについての結論は誘導的になされるので - 私的なものから一般的なものへ。私たちは、地殻の下の地球の正確な組成を知らないので、地球の表面全体を単に地質学的に探検しませんでした。したがって、原子質量の数字は確率的である。今日の人々が持っている知識に基づいています。なぜ科学者はこれを満足するのだろうか?分子物理学の場合にのみより高い精度が必要なので、量の慣例的な計算のために、誤差は無視することができる。しかし、大量の順序の違反は、重要な量の荷電粒子 - 陽子の化学的性質のために発表されます。元素が順番に並んでいるのは陽子の数だけです。
</ p>