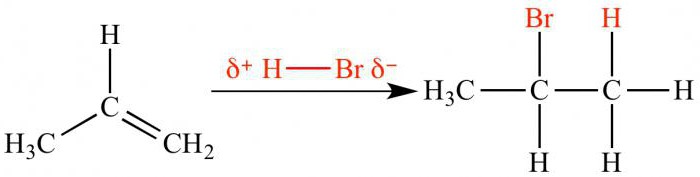
電解解離 - それを理解する方法?
なぜあなたがソリューションは電気を行い、他のソリューションはそうではありませんか?例えば、誰もが、ヘアドライヤーで髪を入れてお風呂に入れないほうがいいということを知っています。結局、水は良好な電流導体であり、作業中のヘアドライヤーが水に落ちると、短絡を回避することはできません。実際には、水はそのような優れた電流導体ではありません。電気をはるかに優れたものにするソリューションがあります。そのような物質は電解質と呼ばれる。これらには、酸、アルカリおよび水溶性塩が含まれる。
電解質 - 彼らは誰ですか?
問題が発生する: なぜいくつかの物質の溶液は、電気、および他を渡す - なし?カチオンおよびアニオン - 荷電粒子の全体のポイント。水に溶解したとき、電解質は、所定の方向に電流移動の作用の下で、イオンに解離します。正に帯電した陽イオンが負極に向かって移動 - 陰極、及び負に帯電した陰イオンは、正端子に移動 - アノード。電離 - 溶融又は水に溶解したイオンへの崩壊剤をプロセスは誇りに思って名前を持っています。
この用語は、スウェーデンの科学者S.アレニウスは電気を通すための解決策の性質を研究しました。これを行うために、彼は物質の溶液を通って電気回路を閉じ、光が来るかどうかを見ました。白熱電球が点灯している場合、溶液は電気を伝導します。これは、この物質が電解質であることを意味します。電球が絶滅している場合、溶液は電気を伝導しないため、この物質は非電解質です。非電解質は、糖、アルコール、グルコースの溶液を含む。しかし、ラストロフの食塩、硫酸、水酸化ナトリウムは完全に電流を流すので、電解解離です。
解離はどのように進行していますか?
その後、電解解離の理論が開発され、ロシア科学者IAによって補完された。 KablukovおよびV.A. Kistyakovskiiは、その実証にD.I.の溶液の化学理論を適用した。メンデレフ大学。
これらの科学者は、電解質酸、アルカリおよび塩の解離は、電解質の水和、すなわち水分子との相互作用の結果として起こる。このプロセスの結果として形成されたイオン、カチオンおよびアニオンは水和され、すなわち密な環でそれらを取り囲む水分子と結合する。それらの特性は、非水和イオンとは著しく異なる。
したがって、硝酸ストロンチウムSr(NO 3)2の溶液および水酸化セシウムCsOHの溶液において、電解解離が進行する。このプロセスの例は、以下の反応式によって表すことができる:
Sr(NO 3)2 = Sr 2+ + 2NO 3 - 、
すなわち、 1つの硝酸ストロンチウム分子が解離すると、1つのストロンチウムカチオンと2つの硝酸アニオンが形成される。
CsOH = Cs + OH-、
すなわち、 1分子の水酸化セシウムの解離により、1セシウムセシウムと1水酸化物アニオンが形成される。
酸の電解解離も同様に起こる。ヨウ化水素酸の場合、このプロセスは次の式で表すことができます。
HJ = H + + CJ-、
すなわち、 1分子のヨウ化水素酸が解離すると、1個の水素陽イオンと1個のヨウ素陰イオンが形成される。
解離のメカニズム。
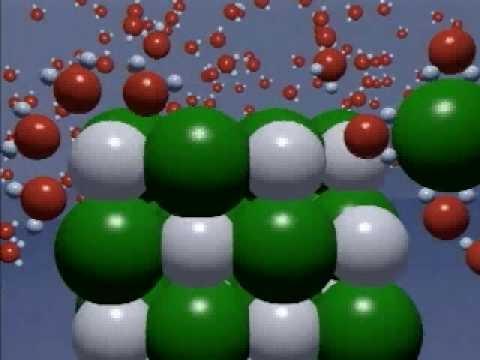
電解質物質の電解解離は、いくつかの段階で進行する。 NaCl、NaOHなどのイオン結合タイプの物質の場合、このプロセスには3つの連続プロセスが含まれます。
最初は、水分子とは異なる2つの水分子(双極子を表す)極(正と負)は、結晶イオンで配向される。彼らは結晶の陰イオンに正の極を、逆も同様に結晶の陽イオンに負の極を付ける。
結晶イオンの水和は水双極子で起こり、
その後、水和したイオンは異なる方向に発散し、電場の影響を受けるまで溶液中を移動し始め、またはカオス的に溶解するように見える。
共有結合性の極性結合を有する物質については、HClおよび他の酸のような、解離の過程は、初期段階で、水の双極子の作用のために共有結合がイオン性になることを除いて同様である。これらは物質の解離理論の要点です。